江西省药品经营企业GSP 监督检查缺陷项目分析
蔡锦尚
江西省药品检查员中心
程一鑫
江西省药品检查员中心
丁若雯
江西省药品不良反应监测中心
熊菲
江西省药品监督管理局
《药品经营质量管理规范》(GSP)于2015 年6 月25 日 公布施行,并根据2016 年7 月13日原国家食品药品监督管理总局《关于修改〈药品经营质量管理规范〉的决定》修正[1],是药品经营管理和质量控制的基本准则。此后,原国家食品药品监督管理总局于2016 年12 月16 日修订印发《药品经营质量管理规范现场检查指导原则》,其中涉及药品批发企业的检查项目及对应的附录检查内容共涉及GSP 的15 个章节,检查项目共计256 项,其中严重缺陷项目(**)10 项,主要缺陷项目(*)103 项,一般缺陷项目143 项;药品零售连锁企业总部按照药品批发企业检查项目检查[2]。
GSP 监督检查是药品监管部门对药品批发企业进行日常监督检查的方式之一。从笔者单位检查情况来看,绝大多数企业运行情况基本符合GSP 要求,检查结论一般为限期整改;极少数企业存在严重违反GSP 的情形,执行停业整改或者立案调查。本文通过汇总分析2021~2022 年期间江西省药品经营企业GSP日常监督检查情况,确定常见的缺陷项目,分析主要问题和原因,并提出相应的解决措施,为进一步提升江西省药品经营企业的质量管理水平提供参考。
1 资料与方法
1.1 资料来源
江西省药品检查员中心在2021~2022 年期间对药品经营企业进行了日常监督检查,共检查企业586 家,覆盖江西省南昌、九江、上饶等11 个地市,涵盖药品批发企业和药品零售连锁企业总部。检查人员重点关注了企业GSP 管理制度、人员素质、设施设备、进货验收、储存、销售、质量管理、信息管理等方面,并通过现场检查、资料核查和询问等方式发现了企业存在的问题。其中,有9 家企业未通过监督检查,日常监督检查通过率约达98.5%。
1.2 调查方法
根据《药品经营质量管理规范现场检查指导原则》,药品批发企业的检查项目涵盖256 项内容,包括总则、质量管理体系、人员与培训、设施与设备、校准与验证、计算机系统、售后管理等15个方面;药品零售连锁企业总部按照药品批发企业检查项目检查。这些条款号码都以5 位数字表示,与GSP 中的具体条款相对应。本文通过使用Excel 工具,统计企业出现的严重缺陷项目、主要缺陷项目、一般缺陷项目和高频次缺陷项目分别对应的GSP 章节内容与频次,为药品经营企业加强质量管理提供参考,同时为药品监管部门提供可行的监督检查措施。
2 缺陷项目情况分析
2.1 缺陷项目总体分布情况
根据江西省697 家次药品经营企业监督检查结果,2021 年1月1 日 至2022 年12 月31 日,笔者单位开展的日常监督检查中共发现问题3147 次。将这些问题按照对应的GSP 章节来划分,其中涉及储存与养护章节的有553 次,设施与设备472 次,人员与培训429 次,质量管理体系文件389 次,收货与验收271 次,校准与验证181 次,组织机构与质量管理职责158 次,计算机系统155 次,运输与配送151 次,质量管理体系136 次,采购116 次,售后管理49 次,销售45 次,出库34 次,总则8 次(表1)。
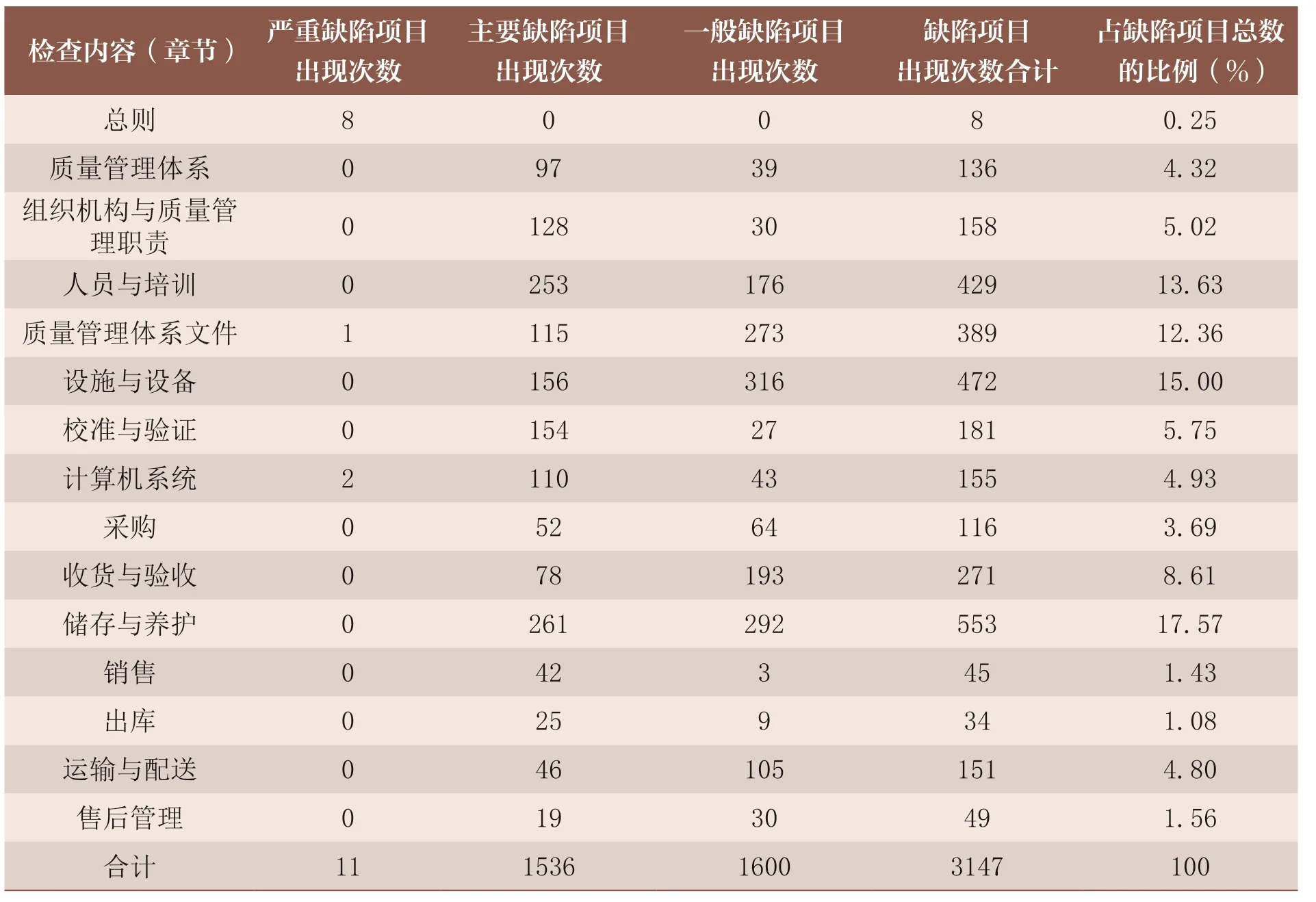
表1 2021~2022 年江西省药品经营企业缺陷项目总体分布情况
2.2 缺陷项目主要分布情况
2.2.1 严重缺陷项目分布情况
监督检查共发现11 个严重缺陷项目,具体情况如下:①《药品经营质量管理规范现场指导原则》总则**00201 规定:企业应当在药品采购、储存、销售、运输等环节采取有效的质量控制措施,确保药品质量,并按照国家有关要求建立药品追溯系统,实现药品可追溯。然而监督检查中发现,某企业使用Excel 办公软件制作“销售出库单(代合同)”单据模板,脱离药品企业资源计划(enterprise resource planning,ERP)系统开具销售单据给下游客户,药品不能保证可被追溯。②总则**00401 规定:药品经营企业应当依法经营。但监督检查中发现,某药品批发企业在未核定的注册地址开展药品经营活动;某企业麻醉药品和第一类精神药品运输证明已过期。③质量管理体系文件**03101 规定:企业制定质量管理体系文件应当完备,并符合企业实际,文件包括质量管理制度、部门及岗位职责、操作规程、档案、报告、记录和凭证等。但监督检查中发现,某药品批发企业的质量管理体系文件不完备,不符合企业实际情况,如存在明显的移植、套用其他企业资料(如文件中存在其他企业或机构的名称、有未处理的模板痕迹等)的情形。④计算机系统**05805 规定:企业计算机系统应当有符合GSP 要求及企业管理实际需要的应用软件和相关数据库。但监督检查中发现,某药品零售连锁企业总部无门店药品请货、收货、养护、验收等数据,无法通过药品ERP系统查询生产采购计划、采购订单。2021~2022 年江西省药品经营企业严重缺陷项目分布情况见表2。
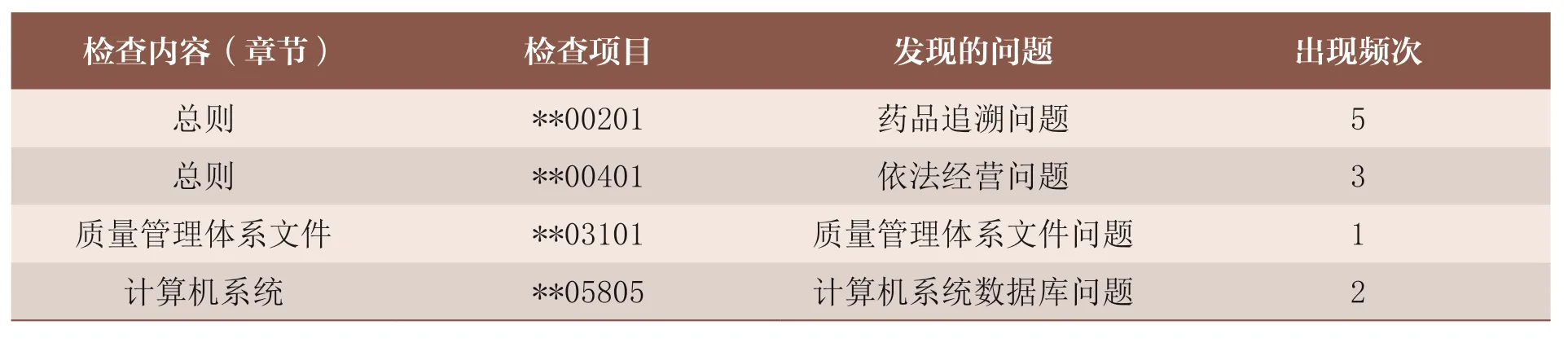
表2 2021~2022 年江西省药品经营企业严重缺陷项目分布情况
2.2.2 高频次缺陷项目分布情况
笔者对日常监督检查发现的缺陷项目进行统计发现,常见问题包括:①根据人员与培训*02701,企业应当按照培训管理制度制定年度培训计划并开展培训和考核,使相关人员能正确理解并履行职责。该检查项目被发现缺陷120 次。②根据设施与设备*04704,库房应当配备自动监测、记录库房温湿度的设备。该检查项目被发现缺陷99 次。③根据人员与培训03001,质量管理、验收、养护、储存等直接接触药品岗位的人员应当进行岗前及年度健康检查,并建立健康档案。该检查项目被发现缺陷85 次。④根据人员与培训*02501,企业应当对各岗位人员进行与其职责和工作内容相关的岗前培训和继续培训,以符合GSP 的要求。该检查项目被发现缺陷82 次。⑤根据质量管理体系文件03501,企业应当保证各岗位获得与其工作内容相对应的必要文件,并严格按照规定开展工作。该检查项目被发现缺陷73次。⑥根据设施与设备04603,库房内墙、顶光洁,地面平整,门窗结构严密。该检查项目被发现缺陷67 次。⑦根据储存与养护*08309,药品与非药品、外用药与其他药品分开存放。该检查项目被发现缺陷64 次。⑧根据计算机系统*05901,计算机系统各类数据的录入、修改、保存等操作应当符合授权范围、操作规程和管理制度的要求,保证数据原始、真实、准确、安全和可追溯。该检查项目被发现缺陷61 次。⑨根据机构和质量管理职责*01710,质量管理部门应当负责指导设定计算机系统质量控制功能,负责计算机系统操作权限的审核和质量管理基础数据的建立及更新。该检查项目被发现缺陷60 次。⑩根据储存与养护*08308,药品堆码垛间距不小于5cm,与库房内墙、顶、温度调控设备及管道等设施间距不小于30cm,与地面间距不小于10cm。该检查项目被发现缺陷59 次。2021~2022 年江西省药品经营企业高频次缺陷项目分布情况见表3。
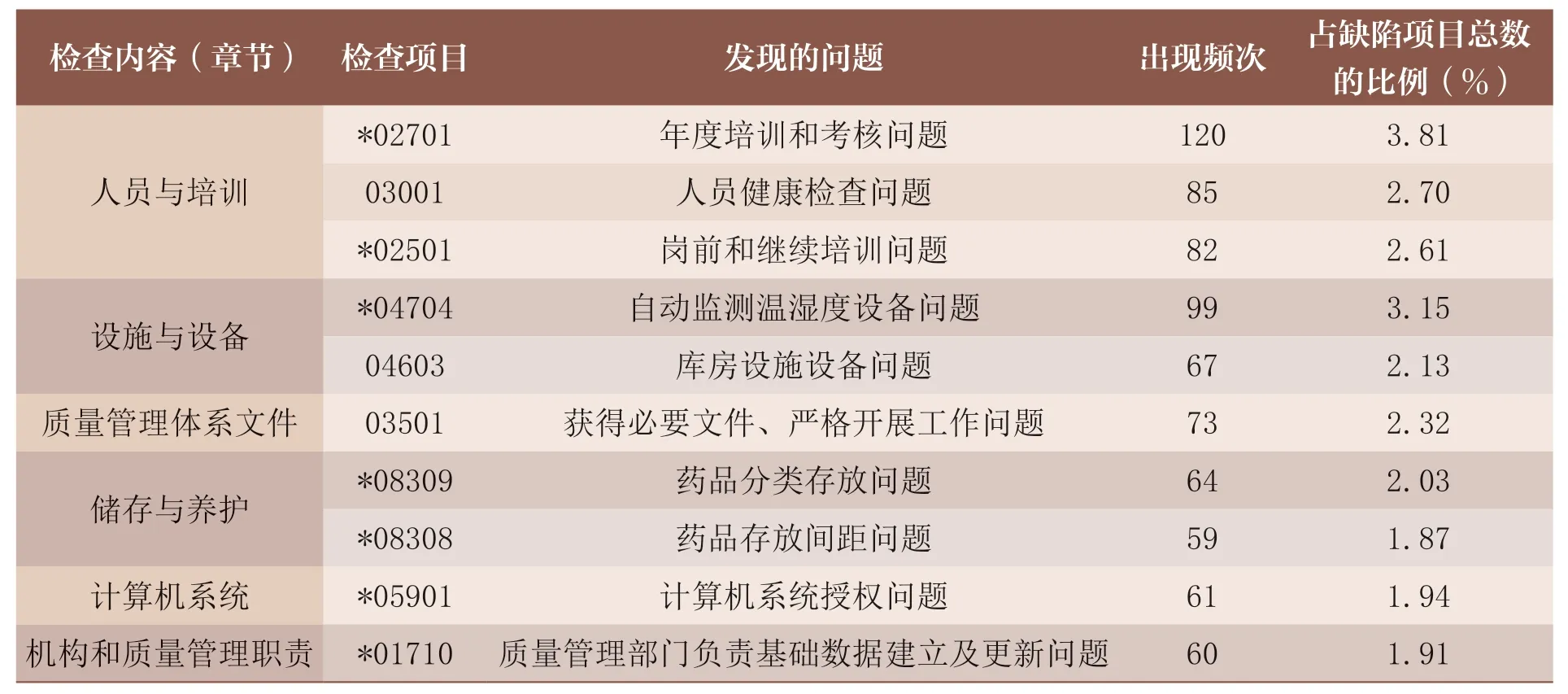
表3 2021~2022 年江西省药品经营企业高频次缺陷项目分布情况
3 药品经营企业存在的主要问题分析
通过对2021~2022 年江西省药品经营企业监督检查发现的缺陷项目进行统计分析可以发现,虽然企业的质量管理意识有一定增强,但GSP 实践和质量管理水平仍有待提高。根据表1 数据,笔者认为相关企业应当重点关注以下4 个方面,并加强相关研究和实践。
3.1 人员与培训
针对该检查项目,监督检查共发现缺陷项目429 次,占缺陷项目总数的13.63%,问题集中表现在:①质量管理人员、验收人员兼职其他业务工作。例如,质量管理人员兼任信息人员工作;验收人员承担收货和养护工作。②岗前培训和继续培训不到位。例如,企业出库复核人员、信息管理部门负责人未进行岗前培训;年度培训中,中药材、中药饮片验收人员未进行中药饮片基础知识相关培训;培训内容无专管药品相关内容。③年度健康检查项目不全或健康档案未归档。例如,部分新入职员工未进行健康体检;部分直接接触药品的员工没有按照规定进行皮肤病和辨色力检查;企业未能现场提供员工2021 年度和2022 年度健康检查资料及健康档案。
3.2 设施与设备
针对该检查项目,监督检查共发现缺陷项目472 次,占缺陷项目总数的15%。由此可见,许多药品经营企业都存在该方面问题,部分企业对设施设备的管理缺乏重视。其中突出问题包括:①仓储条件恶劣。例如,仓库环境非常陈旧,内墙皮脱落、地面不光滑、墙壁渗水,门窗不严密,甚至有蜘蛛网等问题。②设施设备日常维护缺失。例如,有企业在年初就将一年的设备维护记录全部登记完,未能如实记录设施设备的真实使用状况;未定期检查和清洁;未定期对设施设备进行校准等。③设施设备管理较弱。部分企业没有正确设置温湿度系统测点参数,如冷库药品储存温度要求为2~8℃,不少企业将温湿度系统的预警值设置为2~8℃,但由于设施设备存在启动运行的过程,部分药品实际储存温度可能会超过8℃或低于2℃,因此预警值的设置区间应当比2~8℃的区间更窄(如2.2~7.8℃)。
3.3 质量管理体系文件与组织机构和质量管理职责
针对“质量管理体系文件”与“组织机构和质量管理职责”检查项目,监督检查共发现缺陷项目547 次,占缺陷项目总数的17.38%。质量管理体系文件方面,问题集中表现在:企业部分工作人员没有获得本岗位职责、操作规程等相关必要文件,凭借经验做事,未严格按照规定要求开展工作;部分制度文件、表格等没有被编号或加盖受控章;企业未能根据国家药监局下发的最新文件要求,定期审核和修订企业内部文件,甚至部分过时或无效的文件仍然出现在办公场所,未被及时回收处理。组织机构和质量管理职责方面,问题集中表现在:部分企业没有认真考虑如何提高产品质量,也没有监督各部门工作人员遵守相关法律法规。此外,部分企业没有提出有效方案确保计算机系统的安全性,也没有规定计算机使用权限,并且没有严格进行电脑软件的维护与升级。
3.4 储存与养护
针对该检查项目,监督检查共发现缺陷553 次,占缺陷项目总数的17.57%,比例最高。问题集中表现在:①药品储存管理混乱。例如,药品未严格按照包装标示条件储存,如部分常温储存药品(10~30℃)储存在阴凉库(0~20℃);部分药品包装标示贮藏条件为不超过25℃密闭保存,但实际储存在常温库中;不同批号的药品混垛堆放在一起;部分药品直接放置在地面或靠墙堆放;特殊药品验收区域存在部分盲区,没有完全在视频监控范围内[3]。②养护人员工作履职不到位。例如,企业温湿度自动监测系统显示冷库温度高于上限,有报警记录,但养护人员未进行有效调控,温湿度自动监测系统报警处理方式中无处理记录;养护人员无对可疑药品进行锁定的计算机系统权限。
4 建议
GSP 旨在为药品经营者指明行为规范,既可以为行为规范的实施奠定基础,也可以为行为规范的实施指明方式。因此,药品经营者必须清楚认识到自身的责任与义务,积极履行自身职责,将GSP 的原则落实到实践当中,从而实现药品安全、可靠、可持续的质量控制。同时,建议药品监管部门在不断完善GSP 日常监督检查的同时,实施长效监管机制,促进药品经营企业合法诚信经营。
GSP 旨在为药品经营者指明行为规范,既可以为行为规范的实施奠定基础,也可以为行为规范的实施指明方式。因此,药品经营者必须清楚认识到自身的责任与义务,积极履行自身职责,将GSP 的原则落实到实践当中,从而实现药品安全、可靠、可持续的质量控制。
4.1 加强监管,不断提高企业主体责任意识
药品GSP 监督检查,一般是药品监管部门根据年度计划开展日常监督检查。除投诉举报外,一般会提前1~2 天通知被检查企业,确认企业关键岗位人员都在岗,避免人员外出影响监督检查的正常开展。企业人员一般都对此非常重视并提前做好迎检准备,因此企业的重大质量风险隐患不易被发现。为更好地保障药品安全,建议加大检查频率,特别是针对受过行政处罚、涉及投诉举报、经营高风险品种的企业,应当防止因监管缺失造成企业管理水平下降。在检查过程当中,监管人员应将发现的企业风险点详细反馈给企业主要人员,使其了解企业在经营过程中存在的问题,督促其在规定时间内全面自查整改。需要注意的是,药品经营质量的提高,仅仅依靠监管部门落实责任是远远不够的,还需要相关企业提高主体责任意识,尤其是要提高企业负责人和企业质量管理部门负责人的质量管理意识,使企业关键岗位人员能够严格遵守药品经营相关法律法规,并严格落实到日常经营质量管理中。
4.2 加强宣贯,不断提高企业全员参与意识
为了进一步加强药品经营企业质量管理,相关企业人员应当充分了解和遵守药品安全相关标准,熟练掌握和开展工作,并对自身工作负责。此外,建议通过首次会议和培训,督促相关企业人员学习和遵守药品相关法律法规,保证企业合法合规经营。日常监督检查的开展,不仅有助于企业负责人等关键岗位人员了解企业存在的不足或问题,也能够让企业员工更好地理解本职岗位要求。为了促进药品经营企业健康发展,建议检查组采取多种措施,包括但不限于各种形式的培训,以增强企业人员的质量观念,使其明白质量的重要性,并始终坚守这一原则,从而推动企业更好地实现整体质量管控。
4.3 加强培训,不断提高企业人员综合素养
优秀人才的招聘及有效培养,可以为企业发展打牢基础。笔者通过开展监督检查发现,部分药品经营企业人员缺乏系统性培训,欠缺质量管理理念,企业开展质量管理培训工作不到位,存在应付或走过场等现象,导致很多员工并不能理解药品质量的重要性,部分企业对员工能力的提升缺乏有效管理,年度培训只是流于形式,应付监管部门检查。这些企业如果在人才储备、培养及健康体检方面均存在缺陷,那么将难以维护自身商业利益。为了解决该问题,相关企业必须加强人才储备,制定严格的招聘标准,以便更好地选拔优秀的候选者。同时,企业应当为员工安排完善的培训课程,帮助他们更好地掌握相关技术,并对其法律法规、专业技术等水平进行充分评估。例如,企业可以对仓储人员进行培训,使其更好地掌握库房的温湿度、区域颜色、安全措施、堆码、分类、特殊管理以及冷链药品的储存技巧。此外,企业还可以为员工安排计算机应用技术培训课程,帮助他们更好地完成日常生产任务。为了保证GSP 的有效实施,还需要使企业员工清楚了解并遵守相关规定,并积极投入到质量管理中。为了保证药品使用者的安全,所有相关工作人员均应定期参加健康体检,包括但不限于:对于负责验收、维修的工作人员,应对其视力、色觉等指标进行检测;对于与生物制品或蛋白质产品有关的工作人员,应在皮肤病、传染病等方面提出严格要求。
4.4 改善条件,不断提高企业仓库管理水平
药品在经营、运输、储存等环节对温湿度均有一定的要求。就药品经营企业而言,仓库储存条件、设施设备的校准和验证、养护等工作,对于确保药品质量与安全至关重要。从本文统计的缺陷项目情况可知,企业在储存条件、养护、设施设备校准和验证方面存在的问题较多,表明企业普遍在仓库管理方面相对薄弱。对此,企业应当完善仓储硬件水平,改善药品储存条件。设施设备硬件方面,库房配备安装换气扇、灭蝇灯、遮光帘、捕鼠器等;库房内墙、顶光洁,门窗结构严密,地面平整,最好为不易起灰尘的水磨石地面;在库房外进行装卸、发运等作业时,有应对异常天气影响的措施,如安装遮雨棚或者预留宽敞的作业月台等。药品储存管理方面,一方面,应提高储存人员的能力和水平,储存部门负责人、验收人员、养护人员等岗位人员应为药学等专业技术人员,优先考虑或安排有储存等工作经验的人员,企业质量管理部门负责人应对储存岗位人员采取不定期、随机现场考核,督促其提高实操能力和水平;另一方面,养护人员应对药品实行色标管理,在相应区域粘贴指示牌:合格药品区、分拣复核区、发货区为绿色;不合格药品区为红色;退货区、验收区、待确定药品区为黄色。堆垛按照药品外包装标示要求进行。药品日常养护方面,坚持预防为主的原则,建议每月对各类养护设备进行检查并记录。对储存的药品每季度检查一次,一般第一个月检查40%,第二个月检查30%,第三个月检查30%。对陈列的零货药品每个月检查一次,如发现疑似药品质量问题,应当及时与质量管理人员联系,暂停销售,杜绝可疑药品售出。

