右美托咪定对腹横肌平面阻滞疤痕子宫产妇剖宫产术后镇痛及胃肠道功能的影响*
吴瑶瑶 柏效志 谢小娟 徐丽颖 张梦露
(河南科技大学第一附属医院麻醉科,河南 洛阳 471003)
疤痕子宫产妇剖宫产主要与胎盘植入、前置胎盘、感染、深静脉血栓、肠道损伤等风险增加有关[1-3]。疤痕子宫产妇的术后疼痛发生率也较普通产妇高,临床上目前主要依靠腰麻行剖宫产手术,术后镇痛以静脉给药为主,常用的有芬太尼、舒芬太尼等,此类药物为阿片类。但大量应用会引起患者尿潴留、恶心、呕吐以及呼吸抑制等,所以在临床上也常常联合其他的非阿片类药物共同使用,达到减少单独使用某类药物造成不良反应的目的,但是仍有部分患者的术后镇痛效果不理想[4-6]。国外相关研究显示,在局麻药物的基础上,联合使用右美托咪定(DEX)可减少局麻药的使用量,表明了联合用药具有促进镇静以及减轻不良反应的作用,且有利于患者的术后恢复[7-8]。国内目前研究表明,DEX与罗哌卡因联合进行腹横肌平面阻滞(Transversus abdominis plane block,TAPB)在剖宫产产妇术后镇痛、镇静方面效果显著,术后恢复佳,安全性高[9-10]。但是国内外目前关于DEX联合TAPB的研究多数集中在DEX的局部使用,同局部应用相比较,静脉给药在药效发挥、起效时间以及镇痛效果方面均较局部用药有更多的优势,而静脉应用DEX联合TAPB用于疤痕妊娠剖宫产术中的研究较少,因此本研究据此展开探讨,拟为探索疤痕子宫剖宫产术后镇痛方案提供更多参考。
1 资料与方法
1.1 一般资料 选择2020年10月—2021年12月在我院行剖宫产术的105例疤痕子宫产妇作为研究对象,采用随机数字表通过简单随机方法将其分为研究组50例和对照组55例。纳入标准:①足月妊娠,择期行剖宫产的疤痕子宫(横切口)经产妇。②年龄20~45岁。③BMI≤30 kg/m2。④ASA II级。排除标准:①有慢性疼痛病史。②腰麻失败无法完成手术。③长期服用阿片类药物或其他的镇痛药物。④合并凝血功能障碍。⑤合并重要脏器功能异常。⑥对本研究相关药物过敏。所有产妇对本研究知情同意。
1.2 方法 两组均在腰麻下行剖宫产手术,麻醉平面上界控制在T6水平,麻醉诱导前,给予研究组泵注DEX(国药准字H20090248,江苏恒瑞医药股份有限公司) 0.5 μg/kg,对照组泵注等量生理盐水,均10 min泵注完毕。手术操作由同一组医师完成,术后连接PCIA泵[舒芬太尼(注册证号H20100123,IDT Biologika GmbH)2 μg/kg+氟比洛芬酯(国药准字H20041508,北京泰德制药股份有限公司)100 mg,锁定时间设置为15 min]。术毕两组均接受双侧TAPB,嘱产妇取仰卧位,确定髂嵴、肋缘、腋中线位置,使用便携超声诊断仪(sonosite,美国),4~12 Hz高频线阵探头,扫描腹壁前侧腋中线位置,获得腹横肌图像后,使用20G局麻针双侧穿刺,通过水分里技术定位腹横肌平面,回抽无血后,注入0.25%的罗哌卡因(国药准字H20050325,广东华润顺峰药业有限公司)60 mL,每侧30 mL。
1.3 观察指标 记录两组术后4、8、12、24、48 h镇痛效果:①采用疼痛视觉模拟评分表(VAS),0~10分,分值越高疼痛程度越重。②BCS舒适度评分(0分:持续疼痛;1分:安静时无痛,咳嗽或深呼吸时疼痛明显;2分:深呼吸或咳嗽时轻微疼痛;3分:深呼吸时无痛;4分:深呼吸及咳嗽均无痛)。③对两组患者进行针对性宣教,指导阵痛需求评估方法,通过无线镇痛智能管理系统记录镇痛泵有效按压次数。自手术结束时起算,记录肠鸣音恢复时间、首次肛门排气时间、首次下床活动时间。胃肠道不良反应发生情况,记录两组患者术后48 d内恶心、呕吐发生情况。

2 结果
2.1 两组一般资料比较 研究组年龄20~39岁,平均(30.24±3.58)岁,体重62~88 kg,平均(70.35±5.12)kg,孕龄38~41周,平均(39.14±1.12)周,平均手术时间(62.35±5.98)min,平均出血量(301.25±45.68)mL;对照组年龄20~40岁,平均(29.88±3.46)岁,体重60~85 kg,平均(70.20±4.78)kg,孕龄38~41周,平均(39.25±1.08)周,平均手术时间(61.58±5.66)min,平均出血量(305.17±43.87)mL。两组一般资料差异无统计学意义(P>0.05),具有可比性。
2.2 两组术后VAS评分比较 两组术后4 h以及术后48 h的VAS评分无显著差异(P>0.05),研究组术后8、12、24 h的VAS评分低于对照组,差异有统计学意义(P<0.05),见表1。
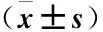
表1 两组术后VAS评分比较
2.3 两组术后BCS舒适度评分 两组术后4 h以及术后48 h的BCS舒适度评分无显著差异(P>0.05),研究组术后8、12、24 h的BCS舒适度评分高于对照组,差异有统计学意义(P<0.05),见表2。
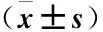
表2 两组术后BCS舒适度评分
2.4 两组镇痛泵累积按压次数比较 两组术后4 h镇痛泵累积按压次数无显著差异(P>0.05),研究组术后8、12、24、48 h的镇痛泵累积按压次数小于对照组,差异具有统计学意义(P<0.05),见表3。
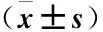
表3 两组镇痛泵累积按压次数比较
2.4 两组肠鸣音恢复时间、首次肛门排气时间、首次下床活动时间比较 研究组肠鸣音恢复时间、首次肛门排气时间、首次下床活动时间均短于对照组,差异具有统计学意义(P<0.05),见表4。
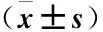
表4 两组肠鸣音恢复时间、首次肛门排气时间、首次下床活动时间比较
2.5 不良反应 研究组与对照组分别有8例和6例恶心呕吐,组间胃肠道不良反应情况无显著差异(P>0.05)。
3 讨论
疤痕子宫剖宫产术后的疼痛主要源自宫缩痛和切口疼痛感,腹部的肌肉、皮肤、腹膜感觉神经主要受T6-L1神经前支支配,上述神经的分支汇聚于腹横肌和腹内斜肌的神经筋膜层,TAPB主要原理是将腹横筋膜平面的脊神经前支阻断,从而使痛觉传导被阻断,缓解腹壁切口的疼痛[11-14]。TAPB虽然对切口痛具有阻断作用,但是对内脏的炎性疼痛的抑制效果不明显。DEX属于高选择性的α2-受体激动剂,在临床上具有较大的应用价值,在镇痛、镇静以及抑制交感神经活性方面均表现出明显的作用,且对呼吸功能的影响较小。相关研究显示,在为手术期输注DEX能明显降低患者手术当天以及术后第1天的炎性因子水平,显著升高IL-10,通过在术后产生炎症的起始阶段发挥作用,缓解炎症反应,对于术后恢复以及肠道功能的恢复均有显著效果[15-17]。
本研究结果显示,两组患者术后4 h及术后48 h的VAS评分、BCS舒适度评分无显著差异(P>0.05),研究组术后8、12、24 h的VAS评分低于对照组,BCS舒适度评分高于对照组(P<0.05)。与Chen等[18]研究结果有所不同,本研究发现,研究组VAS评分在术后8、12、24 h较对照组均明显降低,分析原因,静脉给药的优势在于对患者机体整体发挥作用,镇痛效果更加全面,通过记录镇痛泵的按压次数,还发现,研究组术后8、12、24、48 h的镇痛泵累积按压次数小于对照组(P<0.05)。作为一种佐剂,在区域麻醉中,DEX能够明显延长局麻药神经传导阻滞的有效作用时间,相关机制可能有以下方面:①有相关研究认为,DEX通过在外周直接抑制 Aδ 纤维、C纤维神经信号,对内源性脑啡肽样物质的释放进行调节,从而达到外周局麻镇痛效果[19]。②DEX能作用在外周传入神经纤维部位,将超极化激活的阳离子电流阻断,对神经纤维的动作电位产生抑制作用,使向大脑传递的疼痛信号明显减少,进而发挥镇痛作用。有多项临床试验把DEX作为佐剂用在神经阻滞镇痛中,能使局麻药的感觉以及运动阻滞时间显著延长,阻滞效果明显得到提升,阻滞质量较为满意,在延长术后镇痛时间方面效果显著[20-23]。另外本研究发现,研究组肠鸣音恢复时间、首次肛门排气时间、首次下床活动时间均短于对照组(P<0.05),研究组的胃肠功能恢复情况明显优于对照组,这与Shan等[24]的研究结论一致。分析原因,首先DEX可降低阿片类药物使用剂量,也就减少了药物对肠道功能的负面影响,另外DEX可使中枢α2 肾上腺素能受体激活,使交感神经张力明显降低,还有一个原因可能和DEX能通过增加抗氧化酶活性降低肠道应激损伤程度有关系。
有相关研究显示,DEX可以对肠黏膜中一氧化氮产生抑制作用,进而改善肠道平滑肌部位的微循环,对于改善肠道功能有明显作用[25]。本研究局限性:①样本量小,且仅针对子宫瘢痕妊娠进行研究。②未针对不同浓度DEX的麻醉效果进行分析。③未对实验室指标进行监测评价,仅通过患者主观感受进行评分,可能对结果造成偏倚。在后面研究中,可进行更加全面的评估。
4 结论
DEX联合腹横肌平面阻滞对疤痕子宫产妇剖宫产术后镇痛效果显著,且有助于术后胃肠功能的恢复,安全性高,适合推广。

