模拟高放废物深地质处置条件下Se在铁基材料上的氧化还原行为
许强伟,方 升,刘 晨,龙浩骑,陈 曦,王 波,徐毓炜,周 舵
中国原子能科学研究院 放射化学研究所,北京 102413
随着核能和核技术的不断发展,特别是20世纪中叶以来,人类开发利用核能产生了大量高放废物,高放废物的安全处置问题是制约核能可持续发展的关键因素之一。对高放废物采用深地质处置被公认为是安全、可行的方式[1]。高放废物处置库采用的是“多重屏障系统”设计理念[2-3]。在我国,高放废物的包装容器作为除废物固化体本身外的第一道屏障,其长期安全稳定性对核素阻滞具有重要意义,决定核素迁移的源项。针对不同处置围岩环境,包装容器材料的选择也不尽相同,如芬兰和瑞典,选择铸铁作为包装容器,法国、西班牙和瑞士等国,将碳钢作为备选包装容器材料,比利时和英国等将不锈钢作为备选材料[4]。由此可见,铁基材料是包装容器的重要候选材料。然而,氧化还原敏感元素,如Se、U、Np、Pu等在含铁材料中易发生形态转变,从而影响其溶解性和迁移性[5]。79Se是高放废物的重要成分,其半衰期长(T1/2=2.95×105a)、毒性大、形态复杂,是高放废物深地质处置研究中重点考虑的核素之一。鉴于放射性核素79Se在高放废物地质处置中的重要性,并在现有的实验条件下,本工作拟通过静态批式法研究Se(Ⅳ)和Se(Ⅵ)在铁基材料表面上的氧化还原行为,并对实验数据进行初步分析解读,通过推测机理进一步探讨核素氧化还原过程,从而加深对长寿命裂变产物79Se在深地质处置环境中迁移行为的认识,为我国高放废物地质处置的包装容器选材提供基础数据支持。
1 实验部分
1.1 试剂和仪器
铁基材料(纯铁片/304L不锈钢,规格5 mm×5 mm×1 mm)的化学组成列入表1。铁基材料样品及其化学组成均由盛世达金属材料有限公司提供。Na2SeO4、Na2SeO3,分析纯,国药集团,用以模拟放射性核素79Se;所有溶液均采用超纯水(18.2 MΩ/cm)配制。
DIONEX ICS-300离子色谱仪,戴安有限公司;低氧手套箱,φ(O2)<0.001‰,φ(H2O)<0.005‰,米开罗那有限公司;ML204/02电子天平,精度为0.01 mg,梅特勒-托利多仪器(上海)有限公司;MAIA3扫描电子显微镜(SEM),捷克TESCAN有限公司;XFlash 6160能谱仪(EDS),德国Bruker有限公司;alpha 300拉曼光谱仪,德国WITec有限公司;Milli-Q Direct 16超纯水机,德国默克有限公司。
1.2 实验方法
将实验材料纯铁和304L不锈钢加工成尺寸为5 mm×5 mm×1 mm的样片。铁基材料的面抛光处理、清洗及其与Se(Ⅵ/Ⅳ)的氧化还原实验均在低氧手套箱内完成。对抛光清洗后和无氧腐蚀后的铁基材料分别进行电镜扫描,对腐蚀层进行能谱和拉曼分析。


表2 Se与铁基材料实验条件Table 2 Se and iron-based materials experimental conditions
2 结果与讨论
2.1 Se在蚀前铁基材料上的沉积

图1 蚀前铁基材料在Na2SeO4/Na2SeO3体系中随时间的变化 with time in experimental systems
2.2 蚀前铁基材料反应后的表征


2.3 Se在蚀后铁基材料上的沉积

图2 SQT+Na2SeO3样片(a, c)和SQT+Na2SeO4样片(b, d)能谱点扫SEM图及其对应的Raman谱图Fig.2 SQT+Na2SeO3 sample(a, c) and SQT+Na2SeO4 sample(b, d) energy spectrum point scan SEM image and Raman spectrum

表3 SQT+Na2SeO3样片能谱点扫半定量表格Table 3 SQT+Na2SeO3 sample energy spectrum point scan semi quantitative table

表4 SQT+Na2SeO4样片能谱点扫半定量表格Table 4 SQT+Na2SeO4 sample energy spectrum point scan semi quantitative table

图3 SQG+Na2SeO3样片(a, c)和SQG+Na2SeO4样片(b)的能谱点扫SEM图及其拉曼光谱图Fig.3 Energy spectrum point scan SEM image and Raman spectrum of SQG+Na2SeO3 sample(a, c) and SQG+Na2SeO4 sample(b)
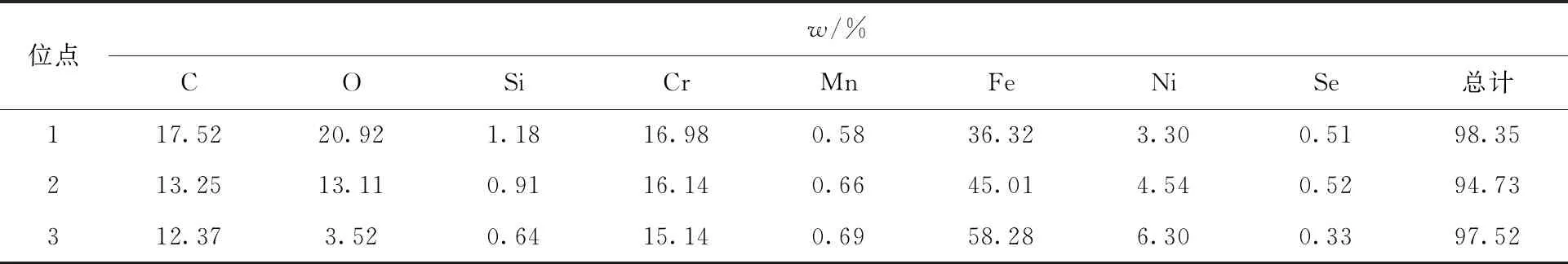
表5 SQG+Na2SeO3样片能谱点扫半定量表格Table 5 SQG+Na2SeO3 sample energy spectrum point scan semi quantitative table
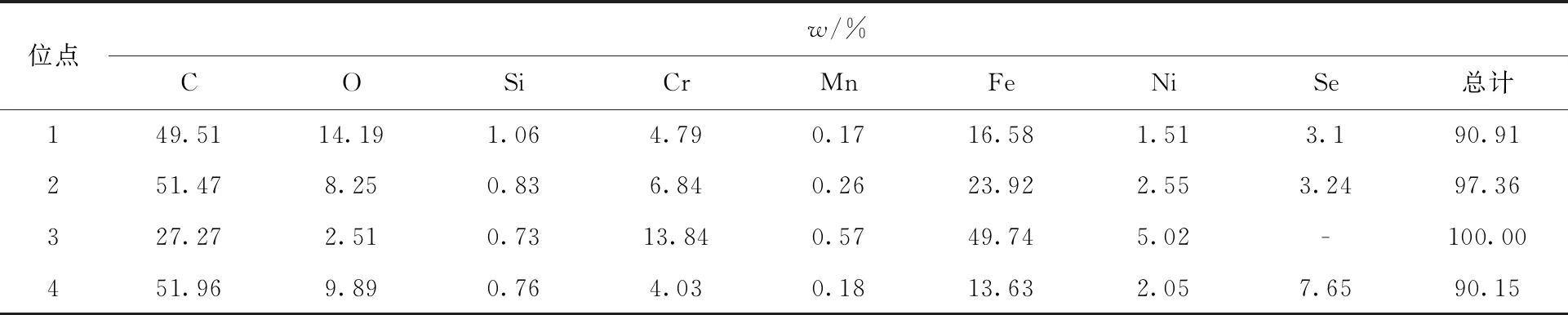
表6 SQG+Na2SeO4样片能谱点扫半定量表格Table 6 SQG+Na2SeO4 sample energy spectrum point scan semi quantitative table

图4 蚀后铁基材料在Na2SeO4/Na2SeO3体系中随时间的变化 with time in experimental systems
2.4 蚀后铁基材料反应后的表征


图5 SHT+Na2SeO3样片(a, c)和SHT+Na2SeO4样片(b, d)能谱点扫SEM图及其对应的Raman谱图Fig.5 SHT+Na2SeO3 sample(a, c) and SHT+Na2SeO4 sample(b, d) energy spectrum point scan SEM image and Raman spectrum

表7 SHT+Na2SeO3样片能谱点扫半定量表格Table 7 SHT+Na2SeO3 sample energy spectrum point scan semi quantitative table

表8 SHT+Na2SeO4样片能谱点扫半定量表格Table 8 SHT+Na2SeO4 sample energy spectrum point scan semi quantitative table


图6 SHG+Na2SeO3(a)和SHG+Na2SeO4(b)样片能谱点扫SEM图Fig.6 Energy spectrum point scan SEM image of SHG+Na2SeO3(a) and SHG+Na2SeO4(b) sample
2.5 Se与铁基材料的氧化还原反应机理
从上述的实验结果和现象,推测在反应体系中发生如下反应。
(1) 在液相中
首先Fe和水中的痕量O2反应生成Fe(OH)2胶体和Fe(OH)3胶体[11-12],如式(1)和(2)。

(1)

(2)
同时Fe(OH)3胶体又可与Fe反应生成Fe(OH)2胶体,如式(3)。

(3)

(4)
(5)
根据式(6)—(8)可以断定反应方程式(4)和(5)是成立的。
E⊖(Fe(OH)3/Fe(OH)2)=-0.56 V
(6)
(7)
(8)
E⊖表示氧化还原电对的标准电极电势,其值越小(例如式(6)中的-0.56 V),其中还原型物质越易失去电子,是越强的还原剂,对应的氧化型物质则越难得到电子,是越弱的氧化剂。反之,E⊖值越大,其中氧化型物质越易得到电子,是较强的氧化剂,对应的还原型物质则越难失去电子,是越弱的还原剂。
此外,Fe(OH)3也会分解生成FeOOH,如式(9)。

(9)
(2) 在固相上

(10)
Fe3O4+2Se↓+4OH-
(11)
(12)
2Fe3O4+Se↓+2OH-
(13)
Se多聚集在铁基材料腐蚀产物上,这与上述面扫结果相对应。
3 结 论


(3) 无论是在Na2SeO4体系中还是在Na2SeO3体系中,腐蚀前铁基材料的反应速率均要快于腐蚀后铁基材料的反应,且反应量更大。

