2021 年中国体外生命支持医疗质量控制报告
国家心血管病医疗质量控制中心专家委员会体外循环与体外生命支持专家工作组
体外膜肺氧合(ECMO)是体外生命支持技术的一种,用于部分或完全替代患者心肺功能,使其得以充分休息,从而为原发病的诊治争取时间[1]。近年来,国内外ECMO 支持的发展突飞猛进,据国际体外生命支持组织(ELSO)统计,自2015 年1 月至2021 年12 月,世界范围内累计62 003 例患者接受了ECMO 支持治疗[2]。
近年来,我国ECMO 支持数量持续快速增长,但ECMO 支持作为一门多学科参与的交叉学科,患者具有病情重、病死率高等特点;同时,由于ECMO 支持是一门新兴技术,医疗人员管理经验相对不足,并且不同地域和级别医院之间存在极大的不均衡。鉴于此,作为高风险、高花费的限制性医疗技术,积极开展全国范围ECMO 支持质量的评价和改进,提高卫生投入的产出效率,争取最佳医疗结局,成为需高度重视和亟待解决的问题。
本篇体外生命支持医疗质量控制报告基于具有良好代表性的全国医疗质量监测数据,通过比较国内不同地区之间的数据差异,分析并展现我国体外生命支持医疗质量的现状。同时,通过比较分析我国与全球注册登记数据的差异,探究影响体外生命支持医疗质量安全的关键环节和主要原因,为制定相应政策提供循证依据。
1 中国ECMO 支持医疗质量控制工作概况
2017 年,国家心血管病中心受国家卫生健康委员会委托,成立国家心血管病医疗质量控制中心,负责国家心血管病质量控制工作。2021 年初,国家卫生健康委员会正式印发《体外膜肺氧合(ECMO)技术临床应用管理规范》及《体外膜肺氧合(ECMO)质量控制指标》,为标定ECMO 支持诊疗质量提供了重要的工具。同时,随着全国医疗质量监测网络趋于成熟,各级医疗质量控制工作逐步深入,医疗质量相关数据不断积累,在国家卫生健康委员会医政医管局的指导下,由国家心血管病医疗质量控制中心牵头,将ECMO 支持技术纳入我国心血管质量监测范围,围绕我国二级以上医院(不包括军队医院)的ECMO 支持相关住院患者进行分析,截取2020 年1 月1 日至2020 年12 月31 日的相关ECMO 支持诊疗数据,分析我国ECMO 支持医疗质量控制情况。
本次医疗报告数据主要来源于医院质量监测系统(HQMS)及全国医疗质量数据抽样调查系统(NCIS)。HQMS 纳入开展心血管病诊疗的1 910 家三级公立医院和2 124 家二级公立医院,共包括10 259 521 例心血管病相关住院患者病案首页数据;NCIS 纳入2020 年抽样调查的1 642 家三级医院和2 868 家二级医院结构性指标数据。数据提取与分类方法见《2021 年中国心血管病医疗质量报告》[3]。
本报告主要包括以下内容:(1)ECMO 支持医疗与质量安全情况:主要分析全国ECMO 支持资源配置情况、医疗服务能力情况,包括ECMO 支持医疗条件、重点病种、住院结局等相关分析;(2)ECMO支持关键质量控制指标分析:主要分析医疗资源配置情况、医疗质量控制指标数据情况,包括整体医疗水平、诊疗过程、诊疗结局情况等相关分析;(3)医疗质量改进研究及工作展望。
2 中国ECMO 支持医疗评价
2020 年NCIS 纳入医院共实施ECMO 支持5 866 例。在开展ECMO 支持的443 家医院中,年ECMO 支持100 例及以上的12 家(2.7%)医院实施了1 969 例(33.6%)。年ECMO 支持10 例以下的310 家(70.0%)医院实施了1 004 例(17.1%)。根据HQMS,2020 年ECMO 支持患者5 318 例;其中,三级医院治疗5 161 例(97.0%);东部2 893 例,中部1 527 例,共占83.1%。这些患者中位年龄54(35,65)岁,女性占33.5%。由于两个数据库纳入医院不同,统计数据也略有出入。
一项来源于NCIS 数据库的横断面研究显示,2018 年ECMO 支持患者共计2 073 例,东部757 例(36.5%),南部411 例(19.8%),中部275 例(13.3%),西南119 例(5.7%),西北91 例(4.4%),东北62例(3.0%),患者中位年龄50(31,63)岁,女性占35.1%[4]。相比发现,尽管ECMO 支持数量在后疫情时代显著增长,ECMO 支持的开展在各个地区间仍然存在极大的不均衡,无论是每百万人ECMO 支持数量,还是能够开展ECMO 支持的中心数量都明显偏向经济发达地区、高收入地区及人口大省。
3 整体质量
3.1 院内结局
分析患者的医嘱离院率、院内死亡率及非医嘱离院率可以发现,2020 年ECMO 支持患者医嘱离院率44.4%,院内死亡率29.1%,非医嘱离院率20.6%;2019 年分别为43.4%、31.2%和19.0%;2018 年分别为51.4%、27.7% 和14.3%[3]。2020 年院内死亡率最高的三个省(自治区、直辖市)为海南(71.4%)、辽宁(54.9%)及天津(49.3%),最低的三个省(自治区、直辖市)为内蒙古(16.7%)、福建(13.7%)及湖南(8.3%);院内死亡和非医嘱离院率最高的三个省(自治区、直辖市)为海南(85.7%)、青海(83.3%)及河北(81.0%),最低的三个省(自治区、直辖市)为陕西(34.2%)、湖南(26.7%)及新疆(25.0%),见图1。
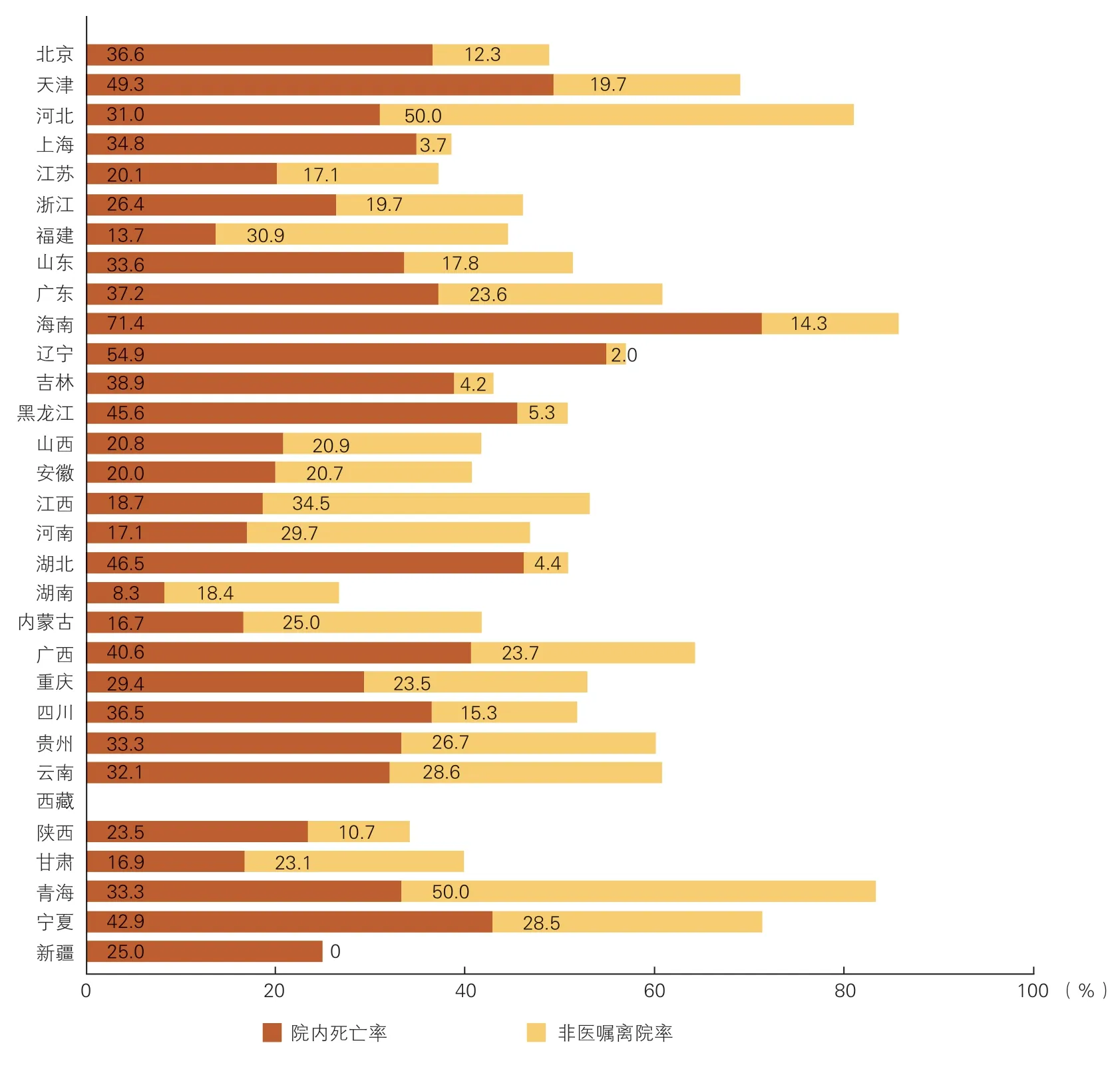
图1 2020 年我国各省(自治区、直辖市)ECMO 支持患者住院结局
3.2 住院时长
2020 年ECMO 支持住院治疗的患者中,平均住院时长为20 d,中位住院时长为14(5,27)d。各省(自治区、直辖市)住院时长存在显著差异,其中江苏的中位住院时长最长,为21(8,43)d(图2)。
3.3 诊疗费用
2020 年ECMO 支持住院治疗的患者中,平均总费用为288 501.7 元,2018 年为271 147.9 元,2019 年为280 976.9 元,住院费用有逐年上升趋势。不同省(自治区、直辖市)间住院费用存在显著差异(图3)。
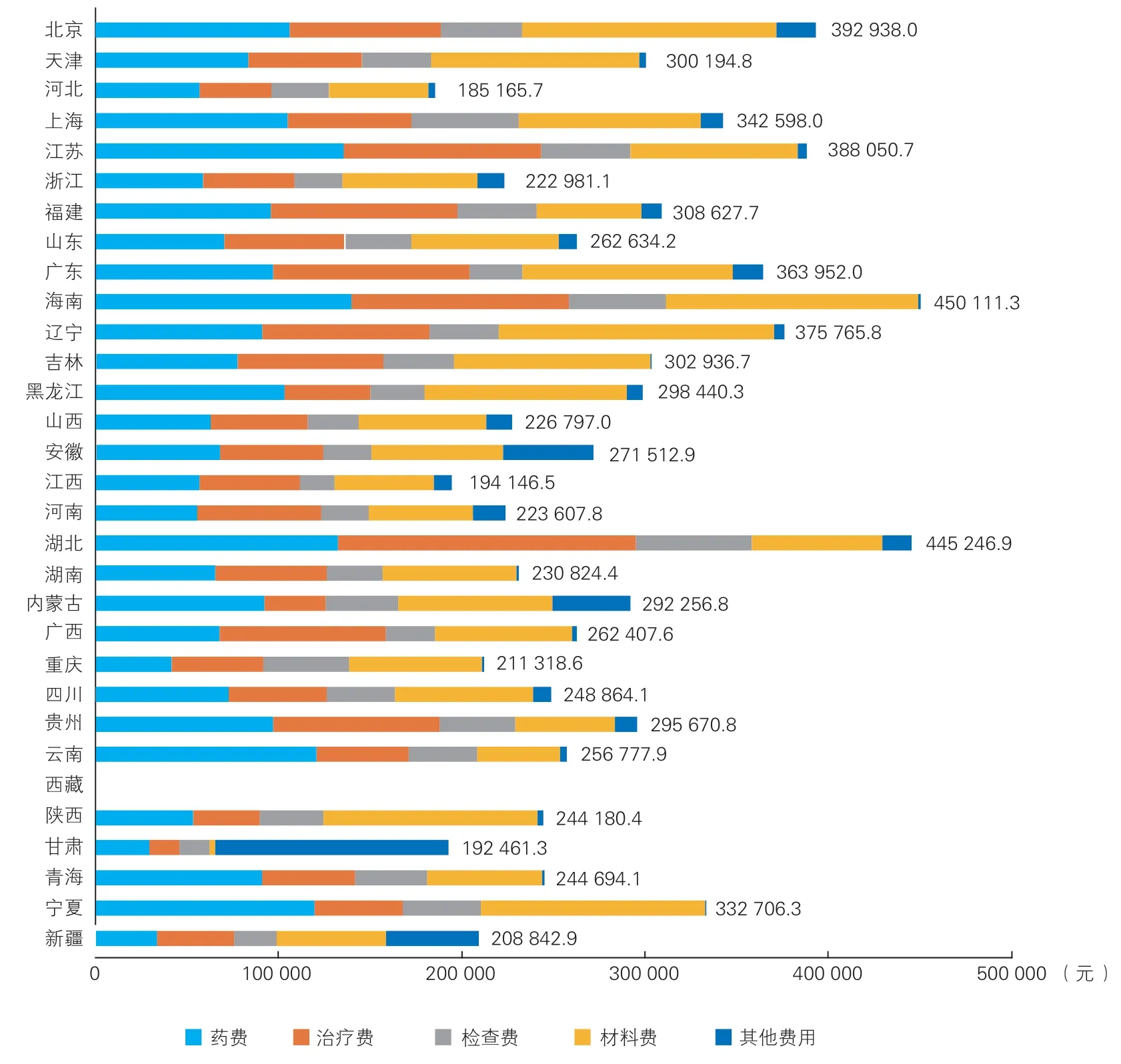
图3 2020 年我国各省(自治区、直辖市)ECMO 支持患者住院费用构成
4 患者特征与诊疗结果
基于HQMS 数据库,并与全球注册登记数据对比,发现患者年龄与原发疾病诊断对ECMO 支持后临床结局的影响较为显著。
4.1 年龄
2020 年我国接受ECMO 支持的新生儿(≤28 d)共192 例,医嘱离院率56.3%;儿童(<18 岁)共343例,医嘱离院率57.7%。与截至2020 年全球注册登记数据相比(表1),我国新生儿及儿科患者占比较低。2020 年我国成人ECMO 支持患者占比为89.9%,而全球注册登记数据成人患者占比仅为44.5%,儿童与新生儿占比分别为21.4%及34.1%。这表明我国儿科ECMO 支持发展与国际水平还存在一定差距,需要进一步明确儿童与新生儿ECMO 支持适应证。

表1 我国ECMO 支持人群和医嘱离院率与全球注册登记数据对比
4.2 原发疾病
根据HQMS 数据库,2020 年接受ECMO 支持治疗的5 318 例患者中,主要仅涉及循环相关疾病的共2 915 例(54.8%),其中47.5%医嘱离院;仅涉及呼吸相关疾病的共525 例(9.9%),其中33.9%医嘱离院;涉及循环及呼吸相关疾病的共1 716 例(32.3%),其中42.8%医嘱离院;主要诊断仅涉及其他疾病的共162 例(3.0%),其中32.1%医嘱离院。所有诊断中包含猝死或休克的患者共2 391 例(44.4%),医嘱离院709 例(29.7%)(图4)。ELSO 统计数据显示,新生儿、儿童及成人患者的循环ECMO 支持出院率为43%、53%、44%[2],我国2020 年统计情况与其相似;呼吸ECMO 支持累计出院率为73%、60%、59%,而我国仅涉及呼吸相关疾病的ECMO 支持患者中仅33.9%医嘱离院。这一方面可能是由于2020 年仍处于新型冠状病毒肺炎暴发初期,患者年龄偏大、合并基础疾病较多、病情变化快,ECMO 支持应用于这一患者群体的适应证不明,导致支持效果不佳[5-6]。

图4 我国ECMO 支持患者中原发疾病诊断及医嘱离院情况
4.3 ECMO 中心
《体外膜肺氧合(ECMO)技术临床应用管理规范》对开展ECMO 培训机构的要求为:“每年完成ECMO 技术临床应用不少于20 例,ECMO 技术成功撤除率达到40%以上”。这也与2014 年ELSO指南中对ECMO 中心规模的建议相符,认为每年ECMO 支持病例数超过20 例的中心患者临床结局优于容量更小的中心[7]。2020 年我国ECMO 支持例数大于20 例且医嘱离院率大于40%的中心共47 家,仅占全部中心的8.9%,医疗质量仍有待提高。同时,在ECMO 支持规模较小的医院中,医嘱离院率更低(图5)。
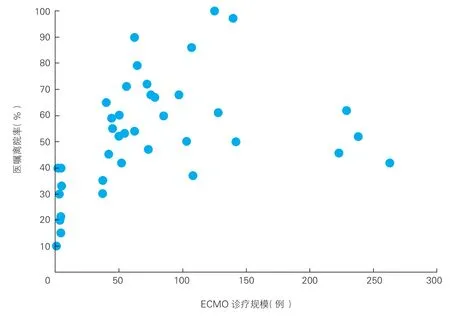
图5 我国医院ECMO 支持诊疗规模与医嘱离院率
5 分析与展望
ECMO 支持自21 世纪初在我国开始应用以来逐步发展,尤其在2019 年新型冠状病毒肺炎暴发后发展迅速,且年度辅助数量仍在持续高速增长。与ELSO 登记数据相比,我国ECMO 支持的总体适应证与术后存活率也在逐步接近国际水平,但部分适应证的把握与儿科ECMO 支持应用规模与国际水平尚有差距。考虑我国潜在的广大医疗市场、不断提高的经济水平和医疗保障能力,国内ECMO 支持未来数年的发展仍有很大潜力。
5.1 目前存在的问题
5.1.1 数据偏离
本次分析发现,小部分医疗中心临床结局与国际或国内既往数据相比出现了显著偏离。部分中心医嘱离院率接近或达到100%,如非刻意错报临床结局,则可能代表适应证把控不严,对无指征患者开展了ECMO 支持;另有部分支持例数较多的中心临床结局反而较差,与实际诊疗水平不符,可能代表着适应证过于激进,对已错过ECMO 支持时机的患者开展了辅助。
5.1.2 数量不均
开展较多ECMO 支持的中心年开展例数超过100 例,但大部分中心年均开展例数不足10 例。通过定期规范化培训将诊断、操作与围术期管理标准化可能是确保医疗质量的必要方法。
5.1.3 信息不全
尚无国家级ECMO 支持质量管理与控制平台,受限于HQMS 及NCIS 系统信息结构与内容,如ECMO 支持模式(静脉-静脉或静脉-动脉)、置管位置(中心置管或外周置管)、置管方法(经皮穿刺或外科手术)、置管地点(院前或院内)及支持时间等部分ECMO 支持关键信息难以获得,降低了统计报告的临床指导意义。另外与已有的其他通过问卷调查获得的类似报告相比,不同统计口径间年度支持数量与死亡率差异较大。推测多种统计手段缺陷共同导致了统计效力降低,例如部分院前急救患者未纳入统计,另有部分病例在转院期间重复进行了统计。
5.2 未来工作重点
5.2.1 提高数据填报数量和质量,形成高质量中国ECMO 支持医疗质量控制报告
一是形成国家中心、省/区域中心和成员单位的三级管理模式,提高各级医疗机构的参与度,提高ECMO 支持质量控制数据填报的数量和质量,全面准确反映我国ECMO 支持开展情况;二是通过质量控制数据平台技术核查、各数据单位数据核查员人工核查及质量控制中心抽查等多种方式,提高填报数据的质量,使得数据内容可靠、可溯源;三是细化医疗质量控制指标的定义和要求,形成标准化操作流程,并定期对相关人员进行培训,确保数据的准确性、完整性和连续性;四是建立完善的ECMO 支持临床质量控制上报系统,包括国际疾病分类(ICD)编码、操作名称、对ECMO 支持置入和撤除操作及时间的准确上报等;五是加强随访管理,制定随访计划,确保患者出院后定期随访,及时填报,实现ECMO 支持的全程管理。
5.2.2 采取切实有效措施,努力提高我国ECMO 支持技术的规范化水平
一是加强各级医院人员ECMO 支持技术工作的培训及继续医学教育,针对临床诊疗不足和失当现象,切实采取针对性措施,以提高ECMO 支持的规范化水平;二是通过定期发布ECMO 支持医疗质量报告,及时反馈各级医疗机构质量控制结果,并开展质量控制结果执行评比及质量控制结果改进评比,提高不同等级医院及不同地区的水平,从而真正提高国家整体ECMO 支持技术水平;三是根据临床情况和国情,更新和优化质量控制指标,对质量控制指标进行更精准管理。
工作组成员名单(按姓氏笔画排序):王伟(上海交通大学医学院附属上海儿童医学中心),王钊(昆明市延安医院),王试福(泰达国际心血管病医院),邓丽(哈尔滨医科大学附属第一医院),卢安东(兰州大学第一医院),叶建熙(厦门大学附属心血管病医院),吉冰洋(中国医学科学院阜外医院),刘宇(北部战区总医院),刘建华(河南省胸科医院),刘晋萍(中国医学科学院阜外医院),刘燕(武汉亚洲心脏病医院),许崇恩(山东省立医院),杜磊(四川大学华西医院),李平(华中科技大学同济医学院附属协和医院),李军(郑州大学第一附属医院),李欣(复旦大学附属中山医院),肖娟(陆军军医大学第二附属医院),杨雷一(阜外华中心血管病医院),宋怡(云南省阜外心血管病医院),武婷(天津市胸科医院),林茹(浙江省儿童医院),金振晓(空军军医大学第一附属医院),周成斌(广东省人民医院),赵明霞(中国医学科学院阜外医院),荣健(中山大学附属第一医院),侯晓彤(首都医科大学附属北京安贞医院),施丽萍(浙江大学医学院附属第一医院),姜福清(中国医学科学院阜外医院深圳医院),洪小杨(中国人民解放军总医院第七医学中心),郭震(上海市胸科医院),啜俊波(哈尔滨医科大学附属第二医院),章晓华(广东省人民医院),梁洛彬(上海德达医院),蒋璇(中国医科大学附属第一医院),程光存(安徽省立医院),廖小卒(中山市人民医院)
数据汇集、分析及初稿撰写人员:高国栋、金泽健、赵明霞、高思哲、闫姝洁、刘晋萍、刘盛、吉冰洋(中国医学科学院阜外医院)
审核、修改及定稿专家:周成斌(广东省人民医院),刘晋萍、刘盛、吉冰洋(中国医学科学院阜外医院)
利益冲突:工作组所有成员均声明不存在利益冲突

