西藏沙棘叶化学成分的研究
赵丽萍,张纽枝,徐福春
(1.西藏职业技术学院,西藏拉萨 850000;2.西藏大学医学院,西藏拉萨 850000)
西藏沙棘叶化学成分的研究
赵丽萍1,张纽枝1,徐福春2*
(1.西藏职业技术学院,西藏拉萨 850000;2.西藏大学医学院,西藏拉萨 850000)
[目的]研究西藏沙棘(Hippophaethibetana)叶中的化学成分。[方法]通过硅胶柱色谱法、Sephadex LH-20、MCI柱色谱法及半制备HPLC研究西藏沙棘枝叶的化学成分,依据波谱数据鉴定其化合物结构。[结果]试验共得到7种化合物:Δ5,22豆甾醇(1),齐墩果酸(2),3′-甲氧基-槲皮素-3-O-β-D葡萄糖苷(3),3′-甲氧基-槲皮素-3-O-a-L-鼠李糖-(1→2)-β-D-葡萄糖苷(4),表儿茶素(5),对羟基苯甲酸丁酯(6),3,4-二甲氧基-5-羟基-苯酚-1-O-α-D-阿拉伯糖-(1→6)-β-D-葡萄糖苷(7);其中化合物1、5、6、7为首次从西藏沙棘中分离得到。[结论]研究可为西藏沙棘资源的综合开发利用提供参考。
西藏沙棘;胡颓子科;沙棘属;化学成分;核磁共振
西藏沙棘(Hippophaethibetana)为胡颓子科沙棘属,别名鸡爪柳,分布于西藏、青海、四川,是一种在高寒地区具有独特经济价值的树种[1]。西藏沙棘拥有发达的根系,主要生长于河漫滩、堤岸和洪积扇,在高寒山区发挥着极为重要的水土保持功能。据研究报道,西藏沙棘的果实内含有丰富的维生素等营养成分,其蛋白质、黄酮类化合物以及种子含油量高于其他沙棘[2]。
已有研究报道指出,西藏沙棘果和叶中的主要化学成分有黄酮类、甾体类及萜类,还有挥发油类、酚类及糖类等化合物[1],其中黄酮类物质在心血管疾病方面有着突出作用,同时还有着改善免疫系统方面的作用。笔者研究分析了西藏沙棘叶中的主要化学成分,为进一步开发利用西藏沙棘天然资源,以及为西藏藏药的开发利用提供科学依据。
1 材料与方法
1.1材料
1.1.1原料及主要试剂。西藏沙棘,采自西藏拉萨地区。主要试剂:甲醇、石油醚、丙酮、氯仿等。
1.1.2主要仪器。Bruker AM-400型核磁共振仪,瑞士Bruker公司;N-1100型系列旋转蒸发仪,上海爱朗仪器有限公司;KQ 3200B型超声波清洗器,昆山市超声仪器有限公司;SHB-III型循环水式多用真空泵,郑州长城科工贸有限公司;WZZ-2S型数字式自动旋光仪,上海精密科学仪器有限公司;WRR熔点仪,上海精密科学仪器有限公司;高效液相色谱仪,美国Waters公司;安捷伦1100高效液相色谱仪;Sunfire Preparative C18色谱柱(10 μm,150 mm,10 mm)。
1.2方法取干燥的西藏沙棘叶3 kg,用甲醇浸泡3次,每次浸泡7 d后,将浸出液过滤,并减压浓缩,得到浸膏,共计60 g。
该浸膏用硅胶拌样,经硅胶柱层析,用石油醚-丙酮(20∶1~1∶1)、氯仿-甲醇(10∶1~10∶2)梯度洗脱,共计得到12个组分。选取其中多个组分通过Sephadex LH-20柱层析,MCI和正相硅胶柱进行组分分离,最后经半制备HPLC纯化,得到纯化合物。
2 结果与分析
该试验在对西藏沙棘叶的分离纯化的过程中,合并类似的样品,得到7个化合物,其含量依次为:1(22.3 mg),2(43.6 mg),3(14.2 mg),4(66.7 mg),5(40.4 mg),6(52.8 mg),7(12.6 mg)。
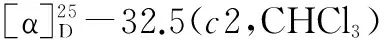
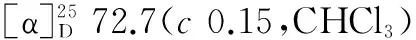
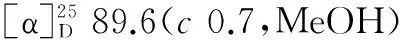
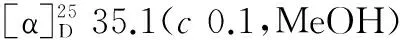
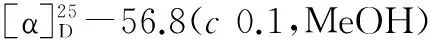
化合物6:淡黄色粉末,化学式为C1H14O3,分子量为194,熔点68~70 ℃。核磁共振波谱数据如下:1H-NMR(CD3OD;400 MHz NMR)δH:7.78(2H,dd,J= 7.8,1.4 Hz,H-3,H-5),7.60(2H,dd,J= 7.8,1.4 Hz,H-2,H-6),4.28(2H,t,J= 6.4 Hz,H-8),1.72(2H,m,H-9),1.42(2H,m,H-10),0.98(3H,t,J= 7.6 Hz,H-11);13C-NMR(CD3OD;100 MHz NMR)δc:163.8(C-1),115.6(C-2),133.9(C-3),122.0(C-4),133.9(C-5),115.6(C-6),168.9(C-7),62.1(C-8),33.5(C-9),21.3(C-10),14.6(C-11)。将波谱数据与文献报道的对羟基苯甲酸丁酯波谱数据[11]进行比较,基本一致,故判定该化合物为对羟基苯甲酸丁酯。
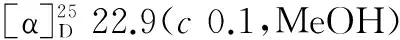
3 结论与讨论
该研究通过硅胶柱色谱法、Sephadex LH-20、MCI柱色谱法及半制备HPLC研究西藏沙棘枝叶的化学成分,依据波谱数据鉴定其化合物结构。共得到7个化合物,其中化合物
1、5、6、7为首次从该植物中分离得到。此项研究首次以西藏沙棘为研究对象,对其化学成分进行了初次研究,明确其化学成分,依据成分相应的理化作用,将西藏沙棘添加进藏药中,为西藏藏药的发展和应用奠定基础,提供了科学依据。
[1] 祁生贵,李莉.RP-HPLC法则定中国沙棘和西藏沙棘枝条中黄酮苷含量[J].青海大学学报,2011,29(2):58-61.
[2] 拉琼,张文驹,欧朗,等.珠穆朗玛峰绒布沟西藏沙棘生境类型及海拔梯度下表型变异[J].应用与环境生物学报,2010,16(2):173-178.
[3] 刘桂艳,郑健,余振喜,等.五叶木通藤茎甾体和三萜成分研究[J].中药,2005,28(12):1060-1062.
[4] 王清吉,王友绍,何磊,等.厚藤Ipomoeapes-caprae(L.)Sweet的化学成分研究[J].中国海洋药物杂志,2006,25(3):15-17.
[5] 冯卫生,王彦志,郑晓珂.中药化学成分结构解析[M].北京:科学出版社,2008.
[6] 张键,孔令义.蒌蒿叶的化学成分研究[J].中国药学杂志,2005,40(23):1778-1780.
[7] 孟江,董晓萍,姜志宏.鲜鱼腥草的黄酮类化合物研究[J].中国中药杂志,2006,31(16):1335-1337.
[8] DASILVA B P,BERNARDO R R,PARENTE J P.Flavonol glycosides from Costus spicatus [J].Phytochemistry,2000,53 (1):872-921.
[9] TERAO J,PISKULA M,YAO Q.Protective effect of epicatechin,epicatechin gallate,and quercetin on lipid peroxidation in phospholipid bilayers [J].Archives of biochemistry and biophysics,1994,308(1):278-284.
Study on Chemical Constituents ofHippophaethibetana
ZHAO Li-ping1, ZHANG Niu-zhi1, XU Fu-chun2*
(1. Tibet Vocational Technical College, Lhasa, Tibet 850000; 2. Medical College of Tibet University, Lhasa, Tibet 850000)
[Objective] To study the chemical constituents in leaves ofHippophaethibetana. [Method] Seven compounds were isolated by silica gel column chromatography, MCI, Sephadex LH-20 column chromatography, and semi-preparative HPLC. [Result] Their chemical structures were elucidated by spectra data analysis. Seven compounds were obtained and identified as Δ5,22stigmasterol (1), oleanolic acid (2), 3′-methoxyl-quercetin-3-O-β-D-glucopyranoside (3), 3′-methoxyl-quercetin-3-O-α-L-rhamnose-(1→2)-β-D-glucopyranoside (4), epicatechin (5), butylparaben (6), 3,4-dimethoxyl-5-hydroxyl-phenol-1-O-α-D-arabinofuranosyl-(1→6)-β-D-glucopyranoside (7). [Conclusion] Compounds 1, 5, 6 and 7 were obtained fromH.thibetanafor the first time.
Hippophaethibetana; Elaeagnaceae;Hippophae; Chemical constituents; NMR
西藏大学青年培育基金项目(ZDPJZK201303)。
赵丽萍(1986- ),女,甘肃张掖人,讲师,硕士,从事农药研究与教学工作。*通讯作者,硕士,从事天然产物研究。
2016-06-12
S 789.4
A
0517-6611(2016)22-075-02

