喹硫平合并碳酸锂治疗伴精神病性症状抑郁症临床对照研究
刘顺发 韦少俊 李 杰 黄善民 黄海燕
抑郁障碍是最常见的心境障碍,以显著而持久的心境低落为主要临床表现,主要分为轻性抑郁症、不伴精神病性症状的抑郁症、伴精神病性症状的抑郁症和复发性抑郁症四种类型。临床上将抑郁症是否伴有幻觉、妄想、阳性思维形式障碍或木僵等精神病性症状分为不伴精神病性症状的抑郁症或伴精神病性症状的抑郁症。由于伴有精神病性症状的抑郁症患者精神障碍程度严重,在使用抗抑郁药物治疗的同时,可合并使用抗精神病药物治疗,近年来文献报道使用非典型抗精神病药物喹硫平、选择性5-羟色胺再摄取抑制剂帕罗西汀治疗抑郁症取得了较好的效果[1],另外,喹硫平联合帕罗西汀治疗难治性抑郁症也取得了较好的效果[2],但由抗抑郁药物引发的躁狂发作在临床上比较常见[3-4]。故本研究通过观察非典型抗精神病药物喹硫平合并心境稳定剂碳酸锂治疗伴有精神病性症状的抑郁症的疗效和安全性以及是否有转躁现象,并与喹硫平合并帕罗西汀治疗伴有精神病性症状的抑郁症进行对照。
1 对象与方法
1.1 对象 为2010年-2011年广西脑科医院住院患者。入组标准:①符合《国际疾病分类(第10版)》(International Classification of Diseases,tenth edition,ICD-10)[5]中伴精神病性症状抑郁症的诊断标准;②年龄18~60岁;③汉密尔顿抑郁量表17项版(Hamilton Depression Scale,HAMD-17)评分>18分;④治疗前血常规、肝功能、肾功能、血糖、血脂及心电图均正常;⑤1年内无酒精或药物依赖者。排除标准:①有严重自杀倾向者、有较严重的器质性疾病者;②哺乳期、妊娠期妇女;③入组前2周内使用过单胺氧化酶抑制剂者、电抽搐治疗者;④服用过喹硫平、碳酸锂、帕罗西汀者。符合入组排除标准共120例,患者及监护人均签署知情同意书。按入院顺序随机分为研究组(喹硫平合并碳酸锂组)和对照组(喹硫平合并帕罗西汀组)各60例。两组均无脱落病例。研究组男性30例,女性30例,平均年龄(28.44±8.43)岁,平均受教育年限(8.47±6.74)年,平均发病年龄(23.41±5.77)岁,平均病程(3.77±4.63)年。对照组男性31例,女性29例,平均年龄(27.98±8.45)岁,平均受教育年限(8.74±6.47)年,平均发病年龄(23.24±5.53)岁,平均病程(3.98±4.26)年。两组患者性别构成、平均年龄、受教育年限、发病年龄、病程差异均无统计学意义(P>0.05)。
1.2 方法 正在接受抗精神病药物治疗的患者入组前停药清洗1周,以排除药物对疗效的干扰。疗程均为8周,均口服给药。喹硫平起始剂量100mg/d,逐渐加至治疗剂量600~750 mg/d,分两次服用;碳酸锂起始剂量500 mg/d,逐渐加至治疗剂量1000~1500 mg/d,分两次服用;帕罗西汀起始剂量20mg/d,逐渐加至治疗剂量40~60mg/d,早上顿服。禁用其他抗精神病药物,失眠者给予地西泮片睡前口服,心动过速者给予普萘洛尔片口服。两组分别于治疗前和治疗第1、2、4、8周采用HAMD、阳性与阴性症状量表(Positive and Negative Syndrome Scale ,PANSS)评定疗效,采用副反应量表(Treatment Emergent Symptom Scale,TESS)评定药物不良反应,于治疗前及治疗第2、4、8周分别检查血常规、肝功能、肾功能、血糖、血脂及心电图,合用碳酸锂者于治疗后每2周检查1次血清碳酸锂浓度。疗效评定由病房主治医师以上人员评定,参加人员先进行培训,经一致性检验,相关系数均>0.85。以HAMD减分率≥80%为痊愈,60%~79%为显著进步,30%~59%为进步,<30%为无效。减分率=(治疗前评分-治疗后评分)/治疗前评分×100%。
1.3 统计方法 使用SPSS11.5进行统计分析。计数资料比较采用t检验,计量资料采用χ2检验。
2 结 果
2.1 临床疗效 研究组痊愈18例(30%),显著进步25例(41.7%),进步14例(23.3%),无效3例(5%),显效率(痊愈+显著进步)为71.7%;对照组痊愈21例(35%),显著进步26例(43.3%),进步11例(18.4%),无效2例(3.3%),显效率(痊愈+显著进步)为78.3%。两组显效率差异无统计学意义(χ2=0.711,P>0.05)
2.2 HAMD评分比较 两组在治疗前、治疗第1、2、4、8周评分差异无统计学意义(P均>0.05)。两组HAMD评分自治疗第1周开始,均较治疗前下降,差异有统计学意义(P<0.05或0.01)。见表1。
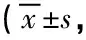
表1 两组HAMD评分比较分)
注:与治疗前比较,aP<0.05,bP<0.01。
2.3 PANSS评分比较 两组在治疗前、治疗第1、2、4、8周PANSS总评分差异无统计学意义(P均>0.05)。研究组PANSS总评分自治疗第1周开始较治疗前下降,差异有统计学意义(P<0.05或0.01),对照组PANSS总分评分自治疗第1周开始较治疗前下降,差异有统计学意义(P均<0.01)。见表2。
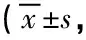
表2 两组PANSS评分比较分)
注:与治疗前比较,cP<0.05,dP<0.01。
2.4 不良反应比较 研究组恶心和胃不适5例,嗜睡5例,头晕4例,口干3例,便秘2例,心电图改变2例,肝功能损害1例,体重增加1例;对照组恶心和胃不适4例,嗜睡4例,头晕3例,口干3例,便秘1例,心电图改变3例,肝功能损害2例,心动过速2例,心动过缓1例。程度都较轻,均能耐受。两组差异无统计学意义(P>0.05)。两组病例8周末均未出现转躁病例。
3 讨 论
喹硫平属二苯西平类化合物,在中枢神经系统中通过对5-HT2A受体的亲和来影响5-HT能神经传递,5-HT2A受体下调是抑郁症状减轻的关键,喹硫平对前额叶皮质5-HT1A受体产生部分激动作用,通过拮抗5-HT2A异质受体,前额叶皮质多巴胺释放增加,发挥抗抑郁作用。本研究初步探讨喹硫平合并碳酸锂治疗伴精神病性症状抑郁症的疗效,前瞻性对照研究8周显示其与喹硫平合并帕罗西汀的疗效相当,显效率分别为71.7%和78.3%(P均>0.05),与鞠红珍等[6]使用利培酮并帕罗西汀治疗伴有精神病性症状抑郁症的显效率82%基本相似。两组病例经过8周的观察,未出现转躁病例,两组HAMD和PANSS在治疗第1、2、4、8周评分差异无统计学意义(P均>0.05)。两组HAMD和PANSS减分均从第1周开始,说明两组均从第1周开始显效。治疗第2、4、8周评分,与治疗前相比差异均有统计学意义(P均<0.01);提示碳酸锂对喹硫平治疗伴精神病性症状抑郁症在本研究中有增效作用。可能是因为碳酸锂影响5-HT摄取、合成、代谢和释放,短期和长期治疗可增高突触体和脑组织色氨酸摄取和含量,因而对大脑5-HT功能有明显加强作用。
喹硫平合并碳酸锂组不良反应以恶心和胃不适、头晕、口干、便秘的发生率较多,头晕、口干与药物拮抗组胺H1等受体有关,多见于治疗开始或增加剂量时,将每日剂量的大部分在睡前服用,可以避免或减轻白天出现的头晕、口干等副作用;便秘与药物抑制肠蠕动有关,一般多吃蔬菜、水果有助通便。两组的不良反应都较轻,均能耐受。提示喹硫平合并碳酸锂安全性好。
有学者认为,伴精神病性症状的抑郁症治疗效果较差,预后欠佳,部分患者转归为双相障碍[4],在抑郁发作的治疗过程中,由抗抑郁药诱发躁狂发作很常见,如何预防转躁,是临床医生面临的一个重大问题。本研究未发现患者有转躁现象,可能是因为喹硫平和碳酸锂均为心境稳定剂,可以预防转躁,值得临床推广。但因本研究样本太小,观察时间较短,有待进一步观察。
[1] 刘顺发,秦霞.喹硫平与帕罗西汀治疗抑郁发作的对照研究[J].四川精神卫生,2010,23(1):11-13.
[2] 王玲,高红,殷志宏,等.帕罗西汀联合喹硫平治疗难治疗性抑郁症对照研究[J].临床心身疾病杂志,2013,19(1):33-39.
[3] 金卫东,陈炯,邢保平,等.抗抑郁药物引发转相的临床流行病学调查(1):转相率及其在不同类型抑郁症中的差异[J].药物流行病学杂志,2005,14(4):217-219.
[4] 金卫东,陈炯,王鹤秋,等.抗抑郁药物引起双相抑郁患者转相的单因素研究及回归分析[J].中国行为医学科学,2007,16(5):416-417.
[5] 范肖冬,汪向东,于欣,等译.ICD-10精神与行为障碍分类[M].北京:人民卫生出版社,1993:103.
[6] 鞠红珍,迟翠玲,梁红蕾.利培酮并帕罗西汀治疗有精神病性症状抑郁症的随机对照研究[J].精神医学杂志,2009,22(3):214-215.

